Иммунные клетки используют NFATc3, чтобы продуцировать окись азота, при бактериальной инфекции
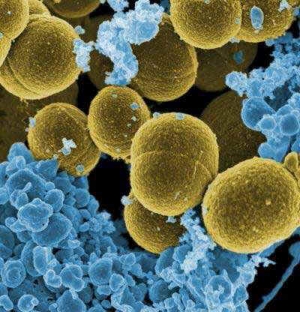 На снимке золотистый стафилококк, устойчивый к действию метициллина. (кликните картинку для увеличения) |
|
||||||||
Белок NFATc3 входит в число регуляторов генов Т- и В-клеток иммунной системы. По словам Рави Раньяна (Ravi Ranjan, сотрудник медицинского колледжа университета Иллинойса, Чикаго), он и его коллеги, работавшие вместе с ним, хотели узнать, выполняет ли NFATc3 какие-либо функции в макрофагах — специализированных клетках-киллерах, уничтожающих клетки бактерий в организме.
Макрофаги уничтожают бактериальные клетки, используя различные химические соединения, такие как окись азота, вырабатывающиеся в ответ на инфекцию. Данные клетки играют важную роль в снижении воспаления при сепсисе — бесконтрольно протекающей реакции на инфекцию, способной привести к повреждениям внутренних органов и гибели.
Когда учёные оказывали влияние на макрофаги, используя сигнальные молекулы, информирующие о бактериальной инфекции, NFATc3, как удалось выяснить, с большей частотой начинал связываться с генами, повышающими продукцию синтетазы окиси азота. Связывание NFATc3 с данными генами предполагает их активацию и, как следствие, усиление продукции оксида азота. Дефицит NFATc3 макрофагов существенно снижал продукцию синтетазы окиси азота.
«Без способности продуцировать индуцибельную синтетазу окиси азота макрофаги потеряли бы ключевой элемент их химического арсенала» — говорит Рави Раньян. По его словам, учёные ожидали, что без способности синтезировать названный выше фермент макрофаги с гораздо меньшей эффективностью способны уничтожать бактерий и устранять сепсис.
Чтобы проверить данную гипотезу, специалисты индуцировали сепсис у мышей, организм которых был лишён способности продуцировать NFATc3. Как и ожидалось, ткани лёгких лабораторных животных были в гораздо большей степени заражены бактериями по сравнению с легочными тканями мышей с индуцированным сепсисом, организм которых был способен синтезировать NFATc3.
«Наше исследование демонстрирует, что NFATc3 нужен макрофагам, чтобы эффективно противостоять инфекции, так как без него данные клетки не способны синтезировать первичный антибактериальный агент — окись азота» — говорит Рави Раньян. По его словам, иммунная система должна найти золотую середину между подавлением инфекции и границами безопасного воздействия на организм, за которые она выходит при сепсисе, причинная вред.
«Сверхпродукция окиси азота может приводить к повреждениям лёгких, даже когда она помогает устранить бактериальную инфекцию» — уточняет Рави Раньян. Ингибитор NFATc3, который можно дать в лекарственной форме пациенту с септическим шоком, способен помочь решить проблему неблагоприятных эффектов, возникающих при сверхпродукции окиси азота.
Более подробное описание результатов проведённого исследования можно найти на страницах Journal of Innate Immunity.
Также по теме:
- Toxoplasma gondii оказывает влияние на поведение человека?
- Выявлена ахиллесова пята бактерий, устойчивых к действию антибиотиков
- Многие жители стран Африки, расположенных к югу от Сахары, не желают проверяться на ВИЧ
- Расширены представления о механизмах защиты сальмонелл от иммунной системы организма хозяина
- Выявлен механизм, который можно использовать в борьбе с гриппом
Источники: