пероксид водорода
Пероксид водорода так же известен под названием перекись водорода. Формула H2O2. Является самым простым представителем пероксидов. По физическим свойствам это бесцветная жидкость. Обладает «металлическим» вкусом. Перекись водорода способна растворяться в воде в неограниченном объёме. Сама является хорошим растворителем. Водный концентрированный раствор пероксида водорода взрывоопасен.Пероксид водорода может служить как восстановителем, так и окислителем. Например, как окислитель он ведёт себя в реакциях с нитритами, окисляя их до нитратов. Как восстановитель – в реакциях с золотом и серебром. Молекула H2O2 сильно полярна.
По причине высокой реакционной способности пероксид водорода способен вызывать в клетках организма окислительный стресс. Обладает бактерицидным действием. В организме млекопитающих отсутствуют ферменты, способные восстанавливать кислород до перекиси водорода.
В силу проявляемых свойств пероксид водорода широко используется для решения различных задач в повседневной жизни. H2O2 в космонавтике применятеся как окислитель ракетного топлива, в медицине – как обеззараживающее вещество, в текстильном производстве – как отбеливатель, в аналитической химии – как реагент для анализа, в промышленности – как катализатор, эпоксидирующий, гидрирующий агент.
Существующие формы выпуска пероксида водорода практически не опасны. Однако сильно концентрированные растворы перекиси водорода при попадании на слизистые оболочки, кожу или в дыхательные пути вызывают появление ожогов.
Последние новости в разделе пероксид водорода
|
09.04.2008 (21:24)
Естественные науки >> Молекулярная биология
Обнаружение пероксида водорода в клетках 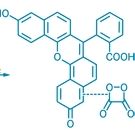 Пероксид водорода накапливается в клетках в результате хронических воспалительных процессов, таких как артрит и порок сердца, поэтому определение молекулы H2O2 в теле является весьма интересным для диагностики и слежения за медицинскими показаниями. Исследователи также заинтересованы в роли H2O2 в клеточном преобразовании сигнала. На данный момент изучаемая трехкомпонентная хемилюминесцентная система может обнаруживать H2O2 в ...>> Пероксид водорода накапливается в клетках в результате хронических воспалительных процессов, таких как артрит и порок сердца, поэтому определение молекулы H2O2 в теле является весьма интересным для диагностики и слежения за медицинскими показаниями. Исследователи также заинтересованы в роли H2O2 в клеточном преобразовании сигнала. На данный момент изучаемая трехкомпонентная хемилюминесцентная система может обнаруживать H2O2 в ...>> |
пероксид водорода, архив по датам
пероксид водорода, архив за текущий месяц
| February 2025 | ||||||||||||||||||||||||||||||||||||||||||
|